Stroombatterijen
De stroombatterij
Een stroombatterij (redox-flow batterij) is een tussenvorm tussen een brandstofcel en een batterij en bestaat uit twee opslagvaten en een reactorvat. Een stroombatterij blijft stroom leveren zolang er nog voldoende elektro-actief materiaal in de opslagvaten aanwezig is. De opgeslagen energie hangt af van de grootte van de opslagvaten. Het grote voordeel van stroombatterijen is dat de capaciteit eenvoudig kan verhoogd door de capaciteit van de voorraadvaten te vergroten. Het vermogen hangt af van het uitwisselingsoppervlak van het membraan en de grootte van de elektroden in het reactorvat. Een verschil met de brandstofcel is dat de voorraadvaten weer gevuld kunnen worden met elektro-actief materiaal door de stroom om te keren en de batterij daarmee weer op te laden. Een andere mogelijkheid om de stroombatterij weer op te laden is het vervangen van de elektrolyten in beide voorraadvaten met nieuw elektro-actief materiaal. Dit is overigens niet mogelijk bij de Zn-Br batterij omdat daar de elektrode in het reactorvat het elektro-actieve element (Zn) bevat.
Typen stroom batterijen
De zink-bromide batterij
Een type stroombatterij is de zink-bromide batterij. Deze batterij bestaan uit twee opslagvaten met een elektrolyt (redoxkoppels) met daarin de materialen die ladingdragers kunnen opnemen of afstaan. Het elektrolyt met het elektro-actieve materiaal wordt, door een reactor, van het ene vat naar het andere vat gepompt. De reactor bestaat uit een elektrolytische of elektrochemische cel met elektroden en een membraan. Tijdens het transport vinden in de reactor aan de elektroden reacties plaats die ladingen afstaan of juist opnemen zoals dat bijvoorbeeld ook gebeurd bij de loodaccu. Het resultaat is dat er een stroom ontstaat in een elektrisch circuit dat, buiten de batterij om, de elektroden met elkaar verbindt. De figuur geeft het voorbeeld van een zink-bromide stroombatterij.
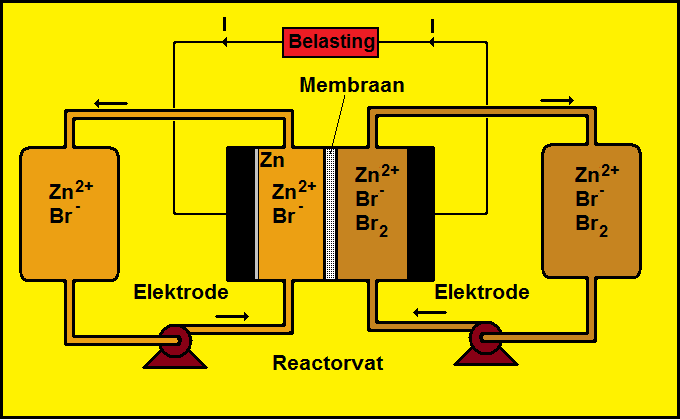
In beide voorraadvaten komen zink (Zn2+) en broom (Br-) ionen voor. In geladen toestand is de negatieve elektrode bedekt met een laag zink (Zn). In het rechter voorraadvat bevindt zich, behalve de ionen, ook een voorraad broom (Br2). Wanneer een elektrisch circuit wordt aangesloten op de elektroden gaat de batterij energie leveren en vindt er in de linkerhelft van de reactor aan de anode de volgende reactie plaats:
Zn → Zn2+ + 2 e-
Het zink aan de elektrode gaat in oplossing onder afgifte van twee elektronen (2 e-). De zinkionen verplaatsen zich door het membraan naar de rechterhelft van de reactorkamer. Het broom in de rechterhelft van de reactor gaat aan de kathode, met opname van twee elektronen, over in twee broomionen:
Br2 + 2 e- → 2 Br-
Broomionen verplaatsen zich van de rechterhelft naar de linkerhelft van de reactor. De elektronen vormen een stroom (I) en leveren dus elektrische energie in het uitwendige circuit van de batterij in een belasting. De ionen worden afgevoerd naar de voorraadvaten waardoor in beide vaten de ionenconcentraties stijgen. De hoeveelheden zink en broom nemen echter af. Wanneer het zink en het broom op zijn is de batterij leeg. Hij kan dan weer geladen worden door een stroom door de batterij te sturen. Dan slaat zink neer op de negatieve elektrode en wordt broom gevormd aan de positieve. Het rendement van deze cel is ongeveer 75%. De Zn-Br-stroombatterij heeft een vermogen tot 1 MW bij een energie van 3 MWh. Door eenheden te combineren kunnen grotere vermogens en grotere energiehoeveelheden worden bereikt [ESA].
Vanadium redox batterij
Naast zink-bromide zijn er stroombatterijen gebaseerd op vanadium, vanadium-bromide en natrium-bromide. Dit type batterij heeft een energiedichtheid van ongeveer 20 tot 35 Wh per kg elektrolyt. Dit is laag vergeleken met bijvoorbeeld lithium batterijen met een energiedichtheid van 80 tot 300 Wh/kg. Er zijn een aantal systemen in bedrijf met vermogens van 5 tot 1500 kW [Wikipedia].
Waterstof stroombatterij
Een breed consortium, met onder andere bedrijven, technische universiteiten en hogescholen, heeft 22 miljoen euro subsidie gekregen voor de ontwikkeling van een lange duur opslagbatterij voor elektriciteit in een waterstofstroombatterij. Dit gebeurt in een project onder de naam SLDBatt-project (Sustainable Long Duration Battery). De waterstofstroombatterij krijgt een vermogen van 1 MWh. Normale lithiumbatterijen hebben een opslagcapaciteit tussen de twee en soms vier uur; de waterstofbatterij krijgt een capaciteit van meer dan tien uur. Een pilot van met een capaciteit van 1 MWh wordt in 2027 geïnstalleerd. Commerciële batterijen krijgen een capaciteit van 15 MWh en groter [Solar365].

